Primeiro teste de anticorpos que possui detecção semi-quantitativa com sensibilidade e especificidade maiores que 99% e auxiliará nos esforços do desenvolvimento de vacinas contra a Covid-19
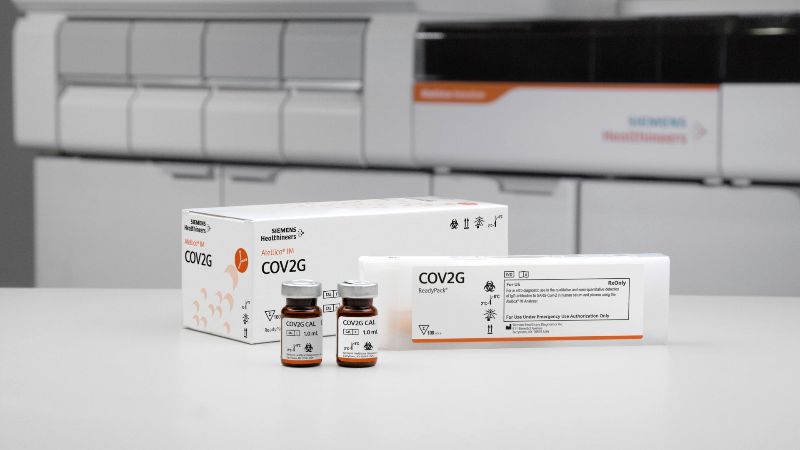
São Paulo, agosto de 2020 – A Siemens Healthineers traz para o mercado o ensaio COV2G, o primeiro teste sorológico para COVID-19 com detecção semi-quantitativa a obter Autorização de Uso Emrgencial pelo FDA. O ensaio oferece 100% de sensibilidade e 99,9% de especificidade, o que é essencial para monitorar com precisão a resposta imune, fornecendo um resultado postivo ou negativo para anticorpos IgG e um resultado numérico em índice. O teste já está disponível globalmente, inclusive no Brasil com registro na ANVISA.
Um resultado positivo ou negativo para anticorpos IgG fornece informações sobre a exposição prévia de um indivíduo ao vírus SARS-CoV-2. É importante ressaltar que, um resultado semi-quantitativo mensurando os níveis de anticorpos IgG linearmente, permite que os médicos interpretem adequadamente o nível de anticorpos IgG na amostra de sangue de um paciente. Com esse valor numérico, os médicos podem estabelecer uma linha de base e estarem melhor preparados para avaliar as alterações da resposta imune de um indivíduo ao vírus. A comparação dos resultados numéricos ajudará na melhor compreensão de como os anticorpos SARS-CoV-2 se desenvolvem em um indivíduo e persistem ao longo do tempo.
Quando um indivíduo é infectado pelo novo coronavírus, anticorpos específicos se desenvolvem em diferentes estágios da infecção. Enquanto o teste de anticorpos totais da Siemens Healthineers – COV2T, detecta os anticorpos IgM e IgG, que estão presentes, tanto precoce quanto tardiamente, durante a resposta imune, o teste de anticorpos COV2G detecta, especificamente, anticorpos IgG, que persistem e são a base para a resposta imune a longo prazo de um indivíduo. A combinação desses testes fornece uma imagem completa do status sorológico do paciente e permite a obtenção de resultados mais precisos para o tratamento clínico completo.
Os resultados altamente precisos dos testes de anticorpos apoiam a tomada de decisões importantes para os pacientes e que podem impactar comunidades. Os testes de anticorpos têm vários usos:
• Como complemento dos testes de PCR para auxiliar na avaliação clínica(³);
• Ajuda na determinação da exposição prévia ao vírus, detectando anticorpos que podem neutralizá-lo(4,5;)
• Identificação de potenciais doadores de plasma convalescente (6);
• Para fins epidemiológicos, incluindo o estabelecimento da prevalência de doenças nas populações;
• Auxiliam a verificação das vacinas à medida que elas se tornam disponíveis(4,5).
O teste de anticorpos COV2G e todos os testes de anticorpos SARS-CoV-2 da Siemens Healthineers foram direcionados para auxiliar nos esforços de desenvolvimento das vacinas, uma vez que detectam anticorpos para S1RBD.A grande maioria das vacinas que estão em desenvolvimento e têm grande potencial de sucesso utiliza a proteína spike, especificamente S1RBD – uma proteína chave na superfície do vírus SARS-CoV-2.
Entre as considerações para a aprovação acelerada da vacina, de acordo com o mais recente Guia do FDA (Food And Drug Administration), emitido em 30 de junho de 2020, o teste sorológico validado em ensaios clínicos pode desempenhar um papel central na avaliação de parâmetros substitutos, como resposta imune a uma vacina. Isso requer entendimento adicional da resposta imune aos SARS-CoV-2 e, especificamente, da resposta à vacina com probabilidade razoável de prever proteção contra a Covid-19 e estudos pós-comercialização para afirmar a eficácia prevista. O teste COV2G atende ou excede os requisitos do FDA(7).
O teste de anticorpos COV2G está disponível em uma ampla base instalada de analisadores, que incluem as soluções Atellica® Solution e ADVIA Centaur® XP e XPT. Testes comparáveis para Dimension® EXL ™ da Siemens Healthineers também estão sendo realizados(8).
A Siemens Healthineers destacou-se durante a pandemia por fornecer ao mercado ensaios sorológicos de alta qualidade. Em uma recente avaliação de quatro testes sorológicos comercialmente conhecidos, conduzida pela Public Health England, em parceria com a Universidade de Oxford, o ensaio COV2T da Siemens Healthineers foi o único teste que atingiu os objetivos de sensibilidade e especificidade (9).
Referências:
1 100% positive percent agreement (sensitivity) at 14 days or more following a positive PCR test.
2 This test has not been FDA cleared or approved. This test has been authorized by FDA under an EUA for use by authorized laboratories. This test has been authorized only for detecting the presence of antibodies against SARS-CoV-2, not for any other viruses or pathogens. This test is only authorized for the duration of the declaration that circumstances exist justifying the authorization of emergency use of in vitro diagnostics for detection and/or diagnosis of COVID-19 under Section 564(b)(1) of the Act, 21 U.S.C. § 360bbb-3(b)(1), unless the authorization is terminated or revoked sooner. Product availability may vary by country and is subject to varying regulatory requirements.
3 https://www.cdc.gov/coronavirus/2019-ncov/lab/resources/antibody-tests-guidelines.html Accessed June 21, 2020
4 Bao L, Deng W, Gao H, et al. Reinfection could not occur in SARS-CoV-2 infected rhesus macaques. Posted 2020 May 1. https://doi.org/10.1101/2020.03.13.990226
5 Cross-neutralization of SARS-CoV-2 by a human monoclonal SARS-CoV antibody. Pinto, D. et al. Nature https://doi.org/10.1038/s41586-020-2349-y (2020).
6 Luchsinger LL et al. Serological Analysis of New York City COVID19 Convalescent Plasma Donors. https://doi.org/10.1101/2020.06.08.20124792.This version posted June 9, 2020
7 Positive percent agreement (sensitivity) ≥ 90%; Negative percent agreement (specificity) ≥ 95%
https://www.fda.gov/media/137698/download. This version posted June 26, 2020
8 Available under IVD CE Mark. Product availability varies by country.
9 Public Health England. Evaluation of sensitivity and specificity of four commercially available SARS-CoV-2 antibody immunoassays. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/898437/Evaluation__of_sensitivity_and_specificity_of_4_commercially_available_SARS-CoV-2_antibody_immunoassays.pdf