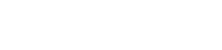Texto Complementar
O QUE SIGNIFICA CONTROLAR A QUALIDADE DO REAGENTE?
Inspecionar: Aceitar ou rejeitar um reagente/ material;
Exemplo: avaliar o reagente no recebimento.
Monitorar: Acompanhar o desempenho do reagente no processo;
Exemplo: avaliar o reagente através do controle interno.
Controlar: Diminuir perdas e retrabalho através do controle interno.
Exemplo: escolha do reagente mais adequado para o perfil da rotina/ cliente.
O controle de qualidade dos reagentes é realizado em duas etapas:
Etapa 1 – inspeção visual;
Etapa 2 – investigação laboratorial.
• 1ª Portaria da Hemoterapia: 1376/93 determina que:
“Os órgãos executores da atividade hemoterápica devem possuir PROGRAMA INTERNO DE QUALIDADE, visando assegurar que os reativos, equipamentos e métodos funcionem adequadamente, dentro dos padrões estabelecidos”
• Resolução 153 de 14/junho/2004 determina que:
Controle de qualidade em imunohematologia:
Reativos: utilizados, armazenados e mantidos de acordo com instruções do fabricante;
No recebimento dos reativos: deve ser realizado controles de qualidade;
Durante a manipulação ou armazenamento dos reativos: deve ser assegurada a integridade dos reativos;
Registrar os resultados obtidos nesses controles;
Devem ser estabelecidas medidas corretivas quando são detectadas anormalidades.
• RDC 57 de 16/12/2010
Art. 9°- Todo serviço de hemoterapia deve ter um sistema de gestão da qualidade no que tange às boas práticas do ciclo produtivo do sangue que inclua a definição da estrutura organizacional e das responsabilidades, a padronização de todos os processos e procedimentos, o tratamento de não conformidades, a adoção de medidas corretivas e preventivas e a qualificação de insumos, produtos e serviços, visando à implementação do gerenciamento da qualidade.
Parágrafo único. O serviço de hemoterapia deve realizar validação de processos considerados críticos para a garantia da qualidade dos produtos e serviços antes da sua introdução e revalidados sempre que forem alterados.
A Portaria Ministerial Nº 1.353 de 14.06.2011 (BRASIL, 2011), determina no Art. 19: O serviço de hemoterapia deve estabelecer um programa laboratorial de controle de qualidade interno e participar de programa laboratorial de controle de qualidade externo (proficiência), para assegurar que as normas e os procedimentos sejam apropriadamente executados e que os equipamentos, materiais e reagentes funcionem corretamente.
Art. 64. Deve haver o controle de qualidade em imunohematologia, considerando os seguintes aspectos:
I – os reagentes devem ser armazenados de acordo com as instruções do fabricante, devendo ser evitada, ao máximo, a permanência do reagente fora das temperaturas indicadas para seu armazenamento;
II – o serviço de hemoterapia deve realizar controles de qualidade em cada lote e remessa recebidos para comprovar que os reagentes estão dentro dos padrões estabelecidos e que não foram alterados durante o transporte;
III – para as análises do controle de qualidade recomenda-se seguir os padrões presentes no Anexo VII deste Regulamento (do controle de qualidade de reagentes de imunohematologia);
IV – no caso de antissoros de origem monoclonal, é indispensável identificação na bula, do clone celular utilizado para produção pelo fabricante;
V – devem ser verificadas, periodicamente, possíveis alterações durante sua manipulação ou armazenamento no serviço de hemoterapia, utilizando protocolos definidos pelo serviço de hemoterapia;
VI – os resultados dos controles devem ser registrados para acompanhamento do desempenho dos produtos; e
VII – devem ser estabelecidas medidas corretivas quando forem detectadas anormalidades.
Parágrafo único. Deve ocorrer, ainda, o controle de qualidade das técnicas empregadas. Para isto, deve-se utilizar sistematicamente, e durante o procedimento técnico, controles negativos e positivos, para confirmar os resultados obtidos.
Boas Práticas e Controle da Qualidade em Serviços que realizam Exames imunohematológicos
Procedimentos padronizados e validados, treinamento, POPs, calibração de equipamentos, controle de qualidade Interno diário, controle de qualidade externo, especificações dos produtos, registros e rastreabilidade, reportar não conformidades, resolução de problemas, planejamento de ações corretivas.
COMO CONTROLAR A QUALIDADE DOS REAGENTES?
A cada lote de reagentes ou remessa recebida, o manual de instruções do fabricante deve ser lido e o controle de qualidade deve ser realizado conforme recomendações do fabricante. Todos os reagentes utilizados na rotina devem ser submetidos ao controle de qualidade antes de ser disponibilizado para uso.
Reagentes: antissoros; hemácias; cartões com gel, enzimas (Bromelina, Papaína); potencializadores (solução de Liss, PEG -Polietilenoglicol), Albumina Bovina à 22%; soros raros e outros reagentes utilizados na rotina diária.
Ao receber o reagente:

Avaliar tecnicamente os regentes para os seguintes parâmetros
Especificidade: Capacidade do reagente em reagir seletivamente. Número de resultados negativos comparando com as amostras verdadeiramente negativas.
Sensibilidade: Limite estabelecido para detecção de reações específicas. Número de resultados positivos, comparando com as amostras verdadeiramente positivas.
Avidez: Intensidade e velocidade com que o anticorpo é capaz de aglutinar (esse parâmetro não tem sido avaliado e a legislação vigente não permite o uso da lâmina para tipagem sanguínea em lâmina)
Reprodutibilidade: Grau de concordância entre os resultados dos testes obtidos.
Estabilidade: Capacidade de um reagente manter inalteradas as suas características.
Os reagentes devem ser validados de acordo com a metodologia indicada pelo fabricante utilizando amostras conhecidas para os controles positivos e negativos.
⇒ Inspeção laboratorial
Os resultados devem estar em conformidade com os parâmetros definidos pela Legislação Vigente.

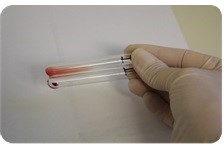

SORO ANTI-A (MONOCLONAL OU POLICLONAL)
O soro anti-A deve reconhecer somente o antígeno A da membrana eritrocitária.
Deve ter reatividade com hemácias A1 de no mínimo 3+, avidez de até 15 segundos, título 256.
Deve ter coloração azul
SORO ANTI-B (MONOCLONAL OU POLICLONAL)
O soro anti-B deve reconhecer somente o antígeno B da membrana eritrocitária.
Deve ter reatividade com hemácias B de no mínimo 3 +, título 256.
Deve ter coloração amarela.
SORO ANTI-Rh (D)
O soro anti-Rh(D) deve reconhecer somente o antígeno D da membrana eritrocitária.
Soro anti-D Monoclonal e/ou Policlonal deve apresentar reatividade de pelo menos 3 + com hemácias de grupo O RhD positivas, título 32.
Não deve reagir com hemácias RhD negativas.
Soro Anti-D salino: deve apresentar título 8 quando testado com hemácias RhD positivas.
REAGENTE CONTROLE DE Rh
Controle de Rh é constituído pelo diluente do soro anti-Rh (D) sem o anticorpo (Anti-D)
Deve ser límpido e não deve reagir com hemácias Rh D positivas ou negativas não sensibilizadas.
Por determinação da Portaria 1353 tem que ser usado em paralelo com o soro anti-Rh(D) como controle negativo.
REAGENTE ANTIGLOBULINA HUMANA
Trata-se de um hetero-anticorpo contra globulinas humanas e/ou frações do complemento.
O reagente deve ter reações positivas de pelo menos 2 cruzes (2+) quando testadas com hemácias sensibilizadas, e negativas quando testado com hemácias não sensibilizadas que apresentem conhecidamente teste de antiglobulina direto negativo.
Não deve apresentar hemólise quando testado com hemácias não sensibilizadas.
REAGENTE CONTROLE DE COOMBS
Suspensão de hemácias humanas de 3% a 5% do grupo O, sensibilizadas por anticorpos IgG, para confirmação de resultados negativos em testes com soros antiglobulina humana.
Deve apresentar reação mínima de 2 cruzes (2+) quando testado frente ao reagente antiglobulina humana mono ou poliespecífica.
ANTISSOROS RAROS
Reagente destinado a fenotipagem eritrocitária com especificidade dirigida para os diversos antígenos eritrocitários.
Estes reagentes devem apresentar reação mínima de 2 cruzes (2+) frente a hemácias que possuam o antígeno correspondente à sua especificidade antigênica e de preferência em heterozigose.
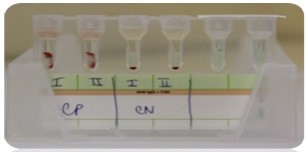
TITULAÇÃO DE ANTICORPOS
São realizadas diluições sucessivas e hemácias com antígeno correspondente ao último tubo que apresentar reação de aglutinação após a centrifugação corresponde ao título do antissoro.
Ex.: Anti-B diluído 1:2, 1:4 …… até 1/512. Se o último tubo a ter aglutinação for o da diluição 1/64, o título será 64.
Análise dos reagentes devem ser registrados em formulário próprio e os reagentes que apresentarem não conformidade devem ser devolvidos ao fornecedor com laudo. Essa é uma boa prática proporcionando uma oportunidade de melhoria para o fabricante do reagente.
CONTROLE DE QUALIDADE DE REAGENTES UTILIZADOS EM EXAMES IMUNOHEMATOLÓGICOS
A seguir são comentadas as questões para as quais foram recebidas mais dúvidas quando disponibilizadas para os usuários Controllab
Pergunta 15: A resposta é a opção 4. Segundo a literatura a microplaca pode ser utilizada para tipagem ABO/Rh em amostras de sangue que sigam os critérios de rejeição e aceitabilidade pré-estabelecidos pelo laboratório.
Nossa experiência mostra que amostras de pacientes que devido a doença de base podem apresentar discrepâncias na tipagem ABO/Rh como: amostras de pacientes que tenham sido submetidos a transplante de medula óssea ABO e ou Rh incompatíveis, pacientes com sepsis, AIDS, mieloma o que pode causar Rouleaux (uma pseudo aglutinação) e outras patologias que podem causar dificuldade na liberação.
Devido ao exposto acima é comum que os Serviços de Hemoterapia utilizem a microplaca preferencialmente na rotina de doadores e para pacientes utilize uma metodologia mais sensível.
Dependendo do perfil das amostras não há impedimento para utilização da microplaca que tratasse de uma metodologia de baixo custo, lembrando que as amostras que apresentarem discrepâncias devem ser submetidas à outra metodologia.
Gabarito
Pergunta 1 – Opção 4
Pergunta 2 – Opção 3
Pergunta 3 – Opção 4
Pergunta 4 – Opção 1
Pergunta 5 – Opção 1
Pergunta 6 – Opção 4
Pergunta 7 – Opção 2
Pergunta 8 – Opção 1
Pergunta 9 – Opção 3
Pergunta 10 – Opção 4
Pergunta 11 – Opção 1
Pergunta 12 – Opção 4
Pergunta 13 – Opção 2
Pergunta 14 – Opção 3
Pergunta 15 – Opção 4
Elaboradora:
Margarida de Oliveira Pinho. Bióloga, Responsável pelo Laboratório de Imunohematologia e Coordenadora da equipe técnica do Serviço de Hemoterapia do Instituto Nacional de Câncer – M.S. – RJ. Especialista em Hemoterapia – Instituto Fernandes Figueira – Fiocruz e em Gestão de Hemocentros – ENSP – Fiocruz – Título de Proficiência Técnica em Imunohematologia pela SBHH.
Referências Bibliográficas:
HARMENING, D. Técnicas Modernas em Banco de Sangue e Transfusão. 4ª ed. – Editora Revinter,2006.
ANVISA, Resolução RDC Nº57 de 16 de Dezembro de 2010
MINISTÉRIO DA SAÚDE, Portaria MS nº1.353, de 13.06.2011